卫健委《原发性肝癌诊疗指南(2026年版)》更新要点
2026 年 4 月 9 日,国家卫健委《原发性肝癌诊疗指南(2026 年版)》 在卫健委的官网发布了 。在正式版发布之后,我将这版指南通读了一遍。与2024年版相比,这里提取了一些值得临床医生关注的更新要点。
预防、筛查和监测
目前,常规的单位体检已经不查乙肝两对半了,这可能会导致一些人对自身的乙肝感染不知晓,从而会延误诊断和治疗,这版指南这样推荐:
建议 18 岁以上人群终生至少进行 1 次乙肝检测。
对于肝癌的超高风险人群(基于 aMAP 及其衍生的标准评估),推荐每 6~12 月进行一次增强磁共振的检查,以避免超声检查漏诊。
肝癌中、高风险人群应至少每隔 6 个月进行 1 次肝癌监测 (证据等级 2,推荐 A);对于肝癌超高风险人群,每隔 6~12 个月进行 1 次增强影像学检查(如增强磁共振成像)加强监测,有助提高早期肝癌检出率。
诊断
对接受过系统治疗和/或局部治疗的肝癌标本,进行病理缓解程度评估,一直是操作难点。新版指南对于 MRP 的 cutoff 数值没有做规定,推荐病理检查时报告存活细胞的确切百分比数值。
明显病理缓解(major pathologic response,MPR):是指在术前治疗后, 瘤床内存活肿瘤细胞减少到可以影响临床预后的阈值以下。目前对 HCC 的 MPR 阈值认定尚不一致, 如有研究显示,以存 活 HCC 细胞≤10%、 ≤15%、 ≤30% 和≤50% 定义 MPR 均与预后相关。为此,建议在诊断 MPR 时注明瘤床存活肿瘤细胞的百分比,便于临床根据肿瘤残留情况制定后续治疗方案。
临床分期和治疗路线图

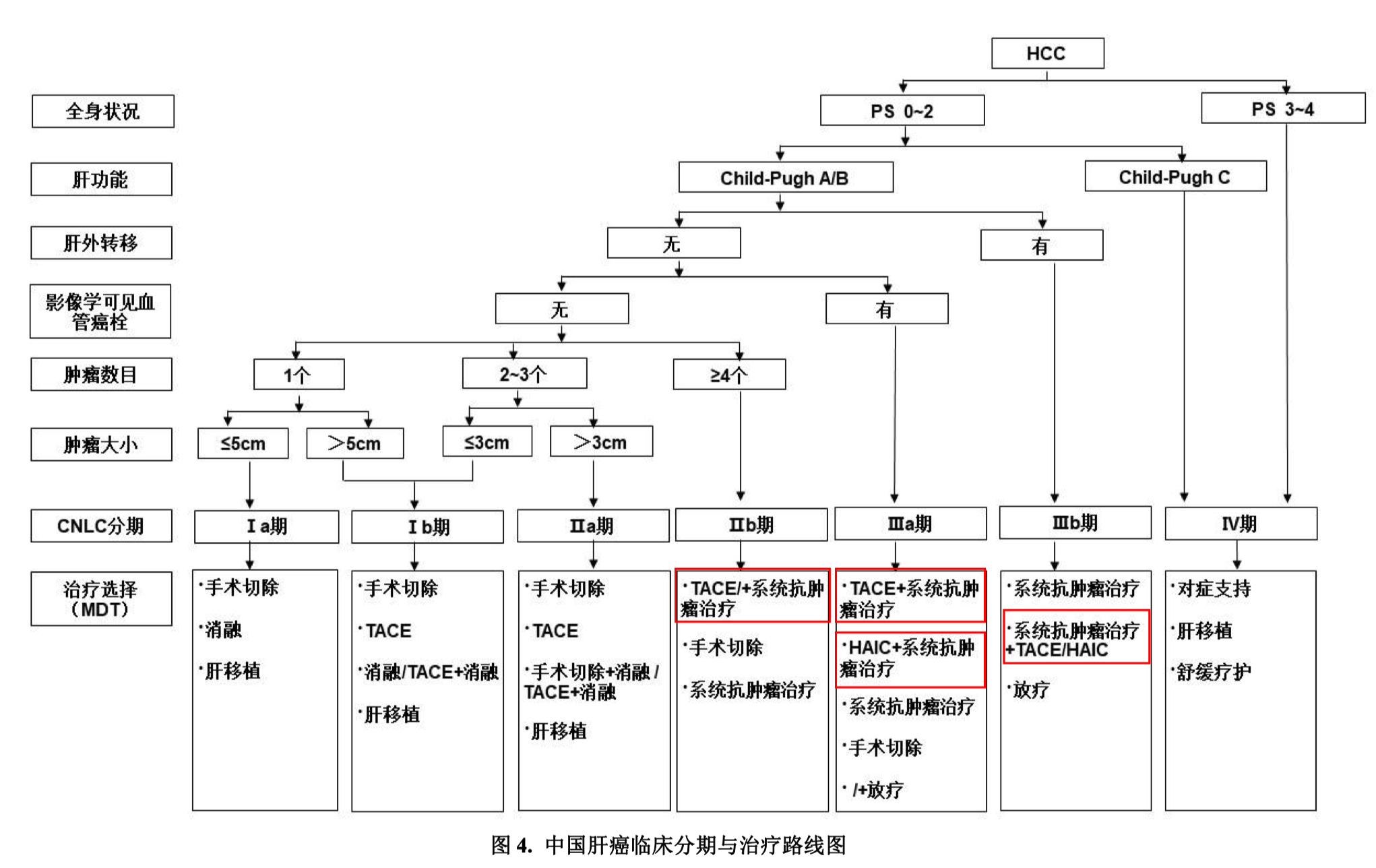
中国肝癌临床分期系统(CNLC)没有变化。
中晚期肝癌的首选或次选治疗方式有一些变化,这是重要更新,值得关注:
- CNLC IIb 期:首选治疗由“TACE”更新为“TACE±系统抗肿瘤治疗”;
- CNLC IIIa 期:首选治疗由“TACE±系统抗肿瘤治疗”更新为”TACE+系统抗肿瘤治疗“;次选治疗增加了“HAIC+系统抗肿瘤治疗”;
- CNLC IIIb 期:首选治疗还是系统抗肿瘤治疗,但次选治疗从“TACE”更新成了“系统抗肿瘤治疗+TACE/HAIC”。
治疗
手术治疗
手术治疗本身,包括适应人群、手术方式和术后随访等等,都没有太多的更新。但是转化治疗、围手术期(或新辅助治疗)领域,有了一些基于随机对照研究产生的 I 类证据,所以做了更新。
对于可切除但伴有高危复发因素患者,新辅助/围手术期治疗可以考虑纳入临床实践,而此前一般建议在临床试验的环境下开展。
近期 CARES-009 研究证实, 对于适合手术切除但具有术后中、高危复发风险的肝癌患者,卡瑞利珠单抗联合甲磺酸阿帕替尼在新辅助及术后辅助的序贯使用,能显著提高患者的无事件生存期(42.1 个月 vs. 19.4 个月, HR=059, P=0.004),同时安全性可控(证据等级 1,推荐 A)。
另外,对于局部晚期(CNLC IIIa 期)的肝癌患者,在系统抗肿瘤治疗有效之后,如果肝内病灶可以切除,手术切除也能带来一定的临床获益。
TALENTOP 研究显示,阿替利珠单抗联合贝伐珠单抗治疗后转化成功患者,相比持续系统治疗,接受肝切除术序贯阿替利珠单抗联合贝伐珠单抗维持治疗 12 个月,可带来具有临床意义的 PFS 提升并呈现 OS 获益的趋势(证据等级 1,推荐 A)。
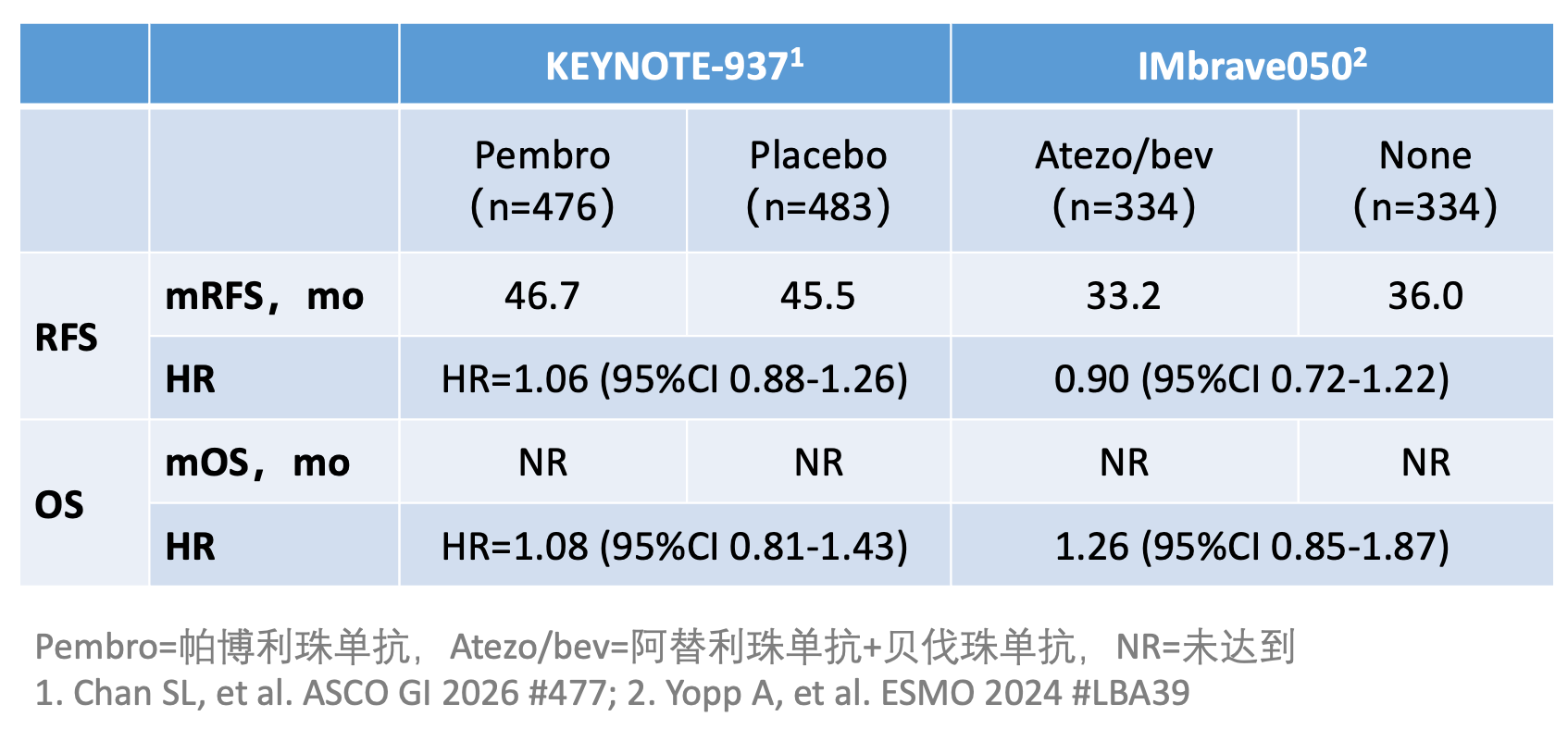
系统治疗用于肝癌术后辅助治疗方面则有了退步。 IMbrave050 研究的期中分析中,阿替利珠单抗联合贝伐珠单抗(T+A 方案)用于肝癌术后辅助治疗时,显示了无复发生存期(RFS)获益,但进一步随访显示 RFS 获益不能维持,且总生存期(OS)也未出现改善趋势。近期的 KEYNOTE-937 研究也显示,PD-1 抗体(帕博利珠单抗)免疫治疗也不能改善 RFS,因此指南不再推荐系统抗肿瘤治疗用于肝癌术后辅助治疗。
在 2024 版中指南中,曾推荐过系统抗肿瘤治疗作为术后辅助治疗:
对于适合手术切除同时具有术后高危复发转移风险的肝癌患者,术后可采取抗病毒、TACE、HAIC、放射治疗、
系统抗肿瘤治疗等辅助治疗以降低术后复发转移率,延长生存时间。
但在 2026 年的新版指南中,去掉了这项推荐。
对于中、晚期肝癌经新辅助/转化后手术以及术后病理明确为中、高危复发的肝癌,目前尚无标准的辅助治疗方案,术后可以尝试采取抗病毒、TACE、HAIC 等辅助治疗以降低术后复发转移率,延长生存。
消融治疗
在射频消融、微波消融、冷冻消融和酒精注射等消融方式的基础上,增加了不可逆电穿孔(IRE) 的论述,但 IRE 应用的证据等级和推荐程度则不及常规的射频消融和微波消融。
经肝动脉介入治疗
- 加入了“优质精细 TACE”和“适度精细 TACE”的论述。
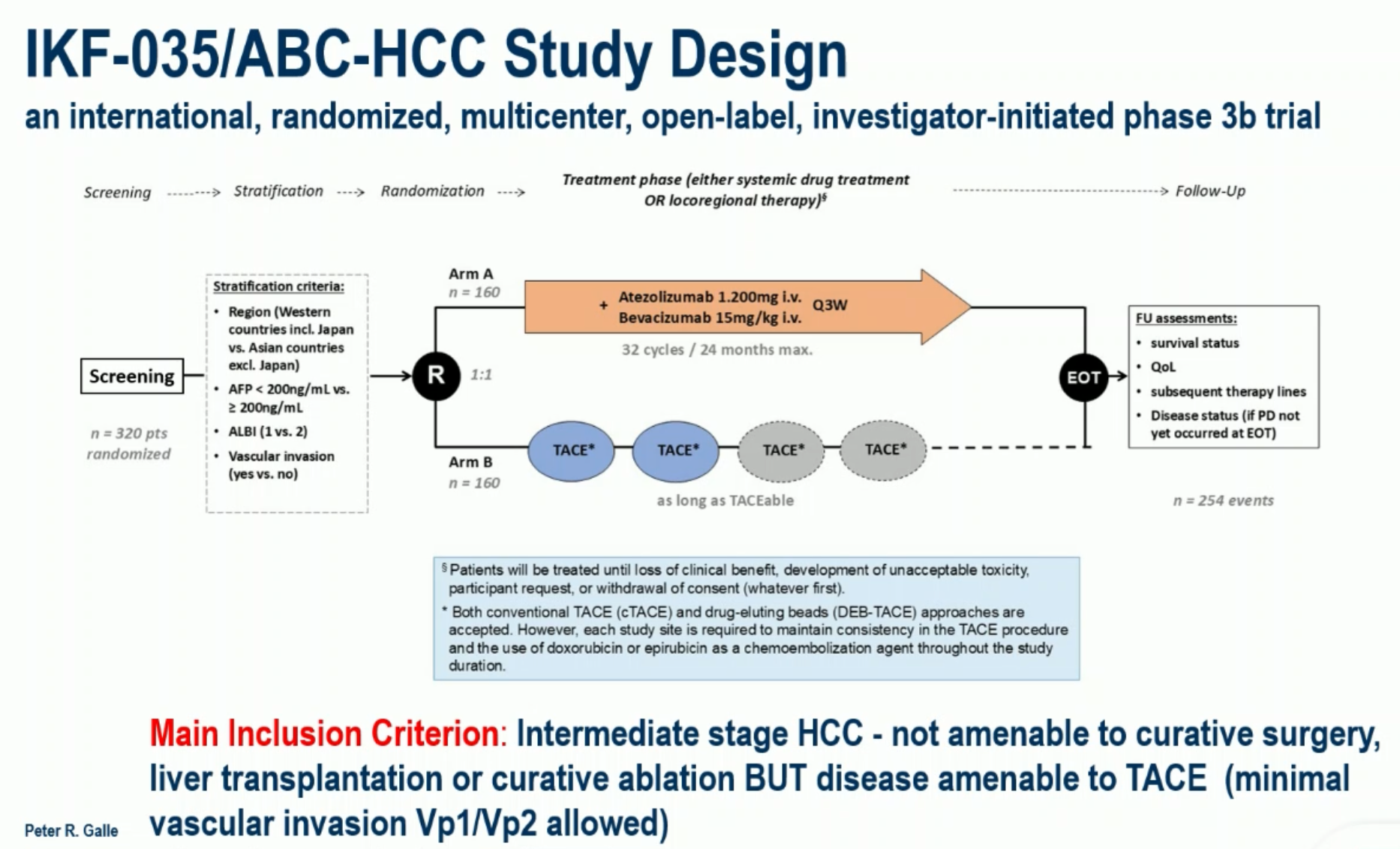
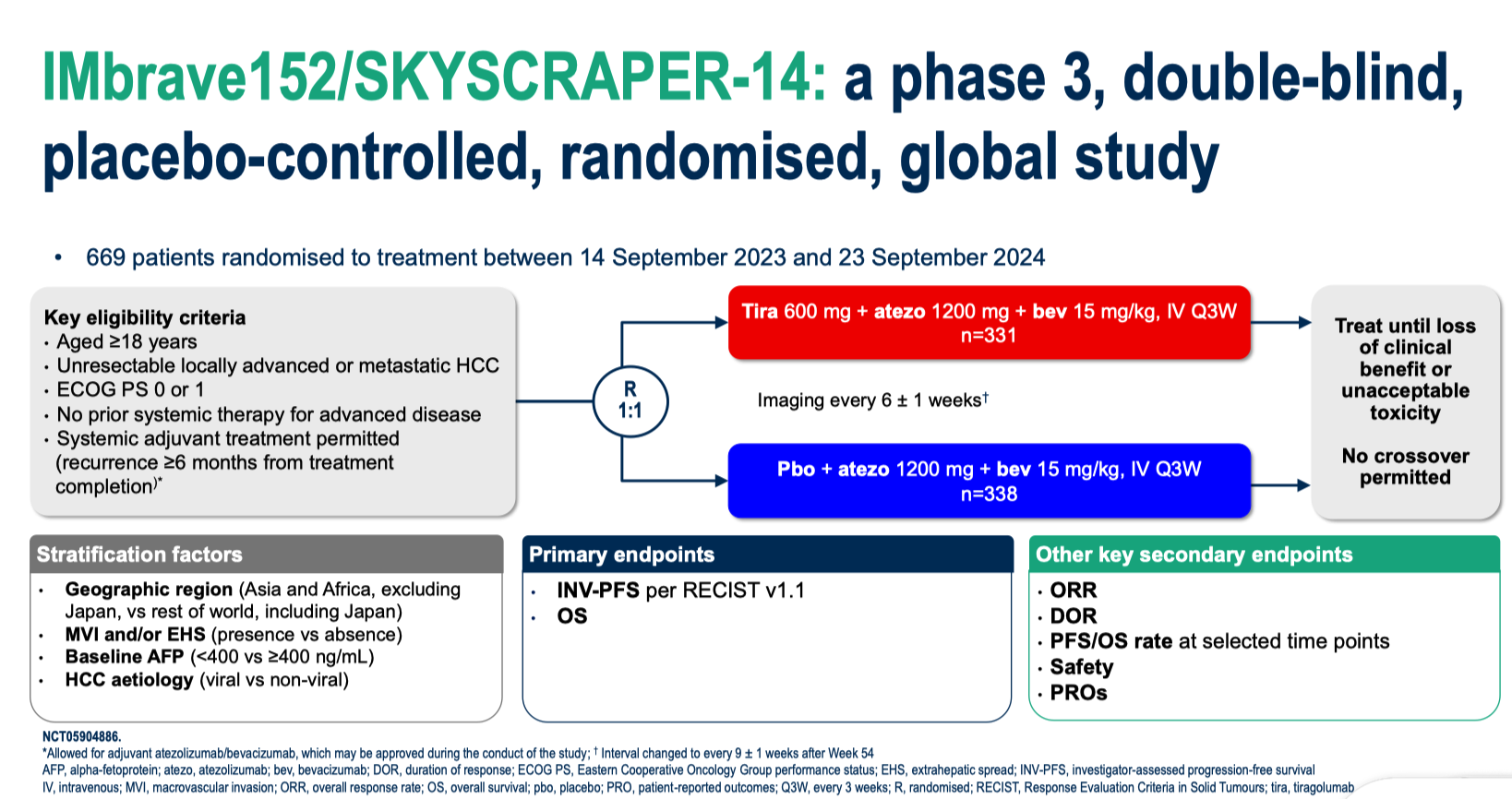
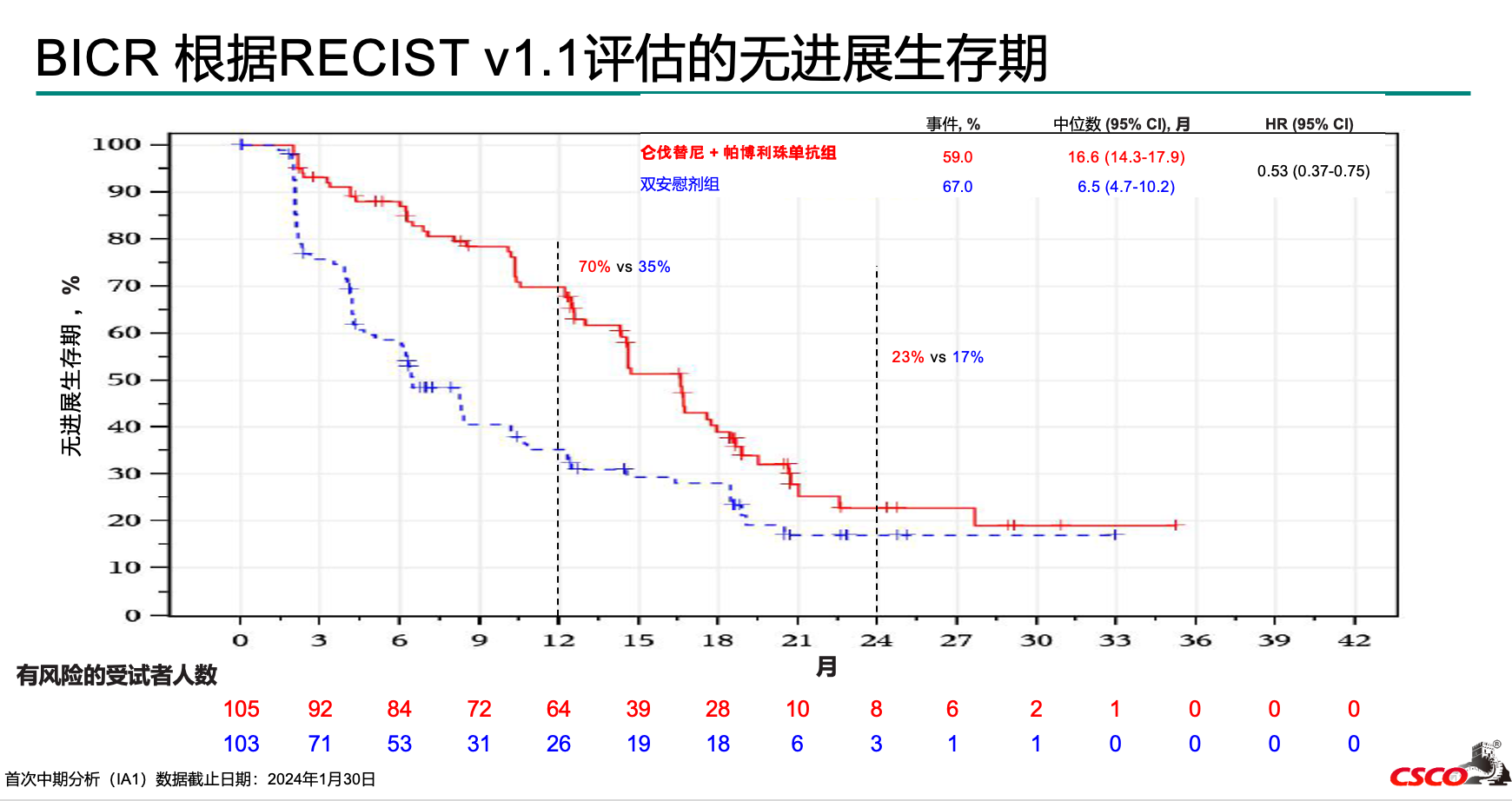
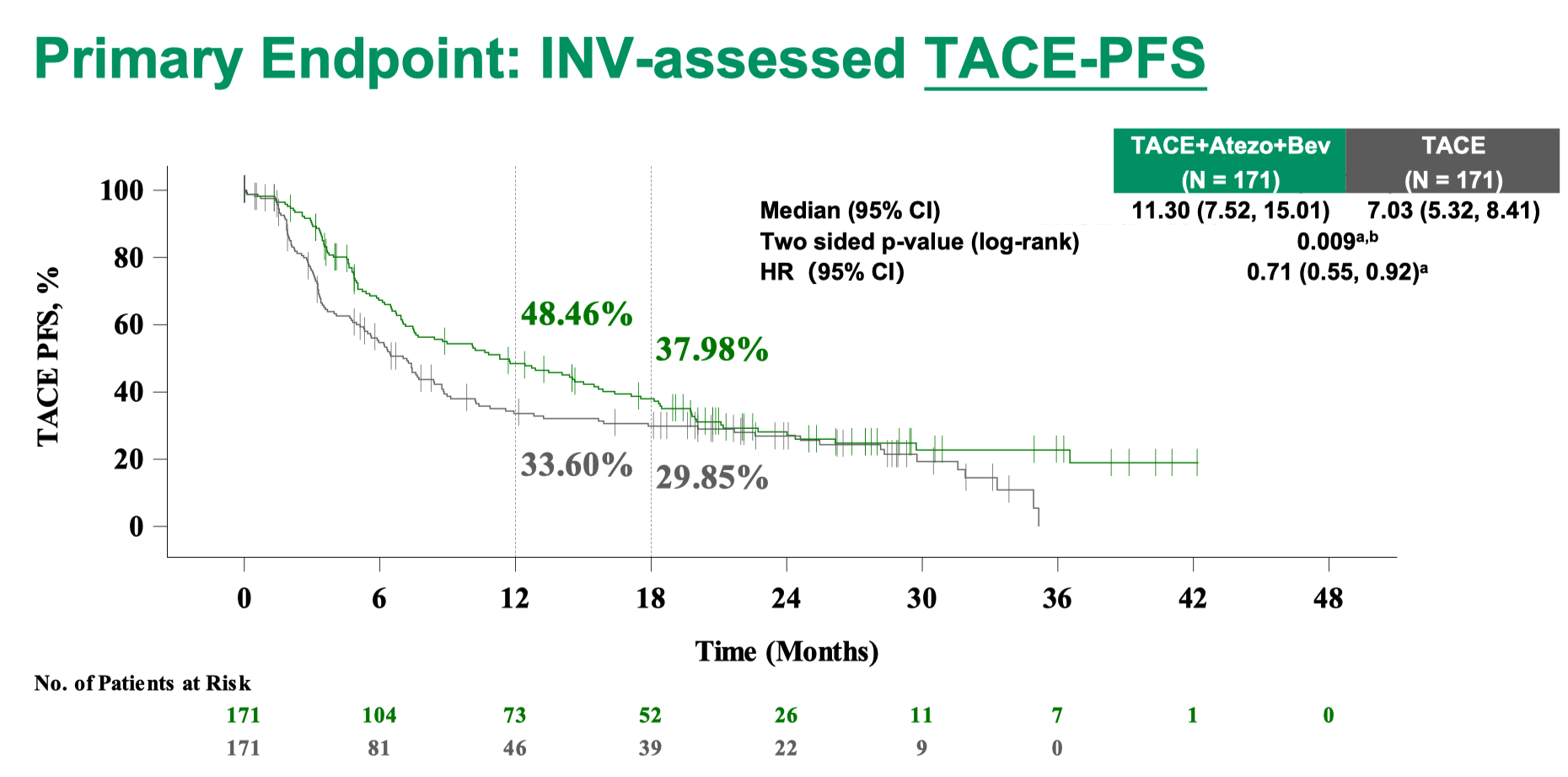
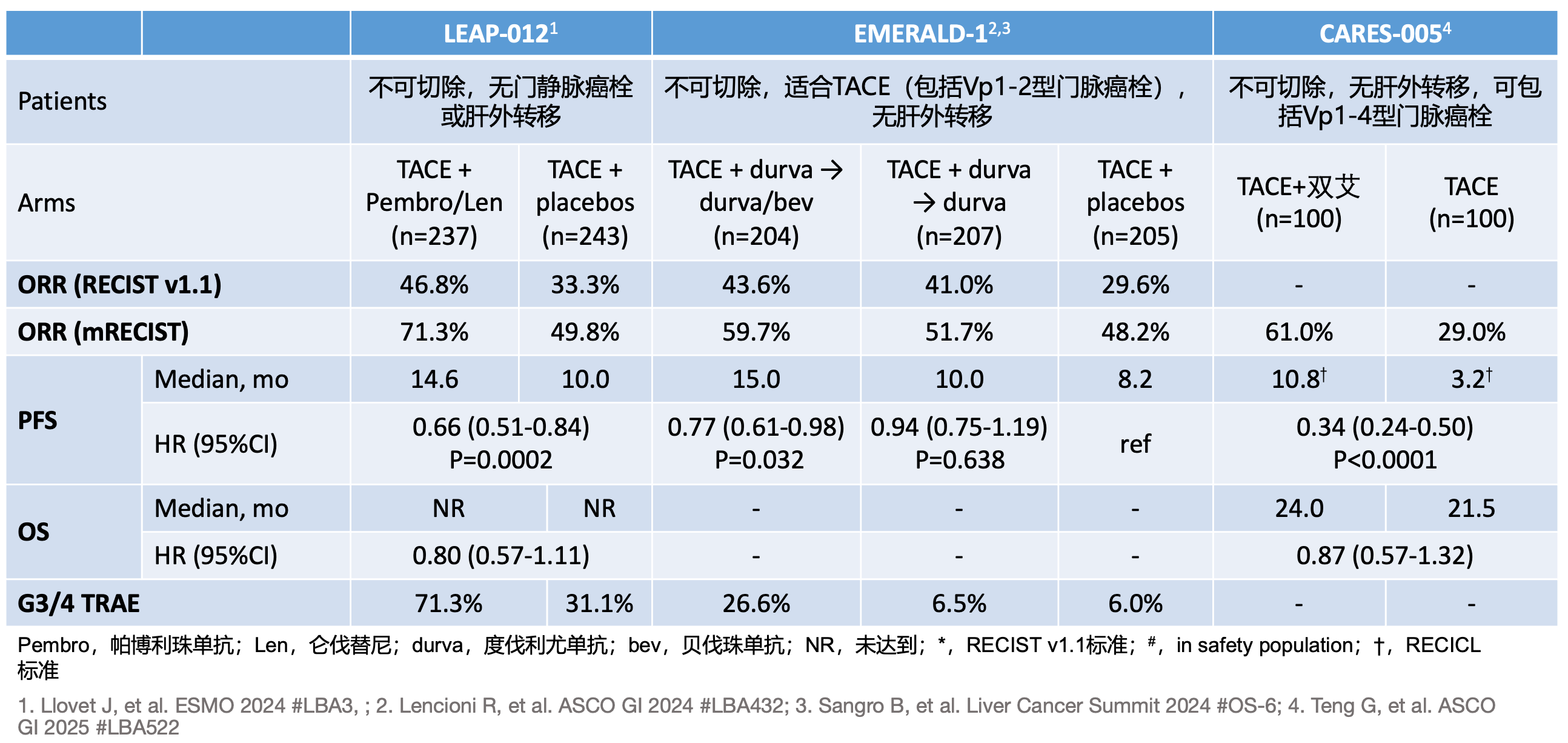
- 增加了 TACE 联合系统治疗的论述,包括 EMERALD-1、LEAP-012、CARES-005和 TALENTACE研究的描述。其中,TACE 联合仑伐替尼和帕博利珠单抗已经在国内获批用于不可切除非转移性肝细胞癌的治疗。也是基于这几项研究的 PFS 和 ORR 获益,但 OS 获益不明朗,CNLC IIb 期患者的首选治疗方式从“TACE”更新为“TACE±系统抗肿瘤治疗”。
- 增加了 HAIC 治疗的细节讨论,包括适应证、禁忌证、操作要点和常见不良反应的处理等信息,要点论述部分对 HAIC 的适应人群做了更新:
2024 年版:mFOLFOX-HAIC 治疗对于多次 TACE 治疗产生抵抗、 肝癌伴门静脉癌栓、肝外寡转移的肝癌患者,疗效优于索拉非尼治疗。
2026 年版:FOLFOX-HAIC 适合于多次 TACE 治疗产生抵抗、 肝内高肿瘤负荷、 肝癌合并主要脉管侵犯或癌栓形成的患者。
- 此外,增加了选择性内放射治疗(SIRT)部分的论述
对于具体的中期肝癌患者,如何根据肿瘤负荷进行分层以灵活应用局部和系统治疗,以避免疗效不足或过度治疗,这里推荐阅读:中晚期肝癌:系统治疗与局部治疗要不要联合?如何联合?
放疗
这部分专业性过强,不做总结。
系统抗肿瘤治疗
一线治疗
最近两年,又有多项系统治疗在国内获批上市,用于不可切除或晚期肝癌的一线治疗。指南也相应地做了更新。目前指南推荐的晚期肝癌一线治疗方案已经有了十来项:
- 免疫联合治疗——目前的优选治疗方案
- 抗血管靶向联合免疫治疗
- 贝伐珠单抗联合 PD-1/PD-L1 抗体,包括:贝伐珠单抗联合阿替利珠单抗(T+A 方案)、联合信迪利单抗(双达方案)、联合特瑞普利单抗(TB 方案) 和联合菲诺利单抗
- 酪氨酸激酶抑制剂(TKI)联合 PD-1 抗体,包括:阿帕替尼+卡瑞利珠单抗(双艾组合) 和 安罗替尼+派安普利单抗(双安组合)
- 双免疫治疗:伊匹木单抗+纳武利尤单抗(O+Y 方案)
- 抗血管靶向联合免疫治疗
- 其他治疗——原文的表述是 “仍然可用于肝癌的一线治疗”
- TKI 单药,包括: 索拉非尼、仑伐替尼和多纳非尼
- 免疫单药:替雷利珠单抗
- 全身化疗:FOLFOX 方案
如何针对具体的患者,在不同的治疗方案之间做出选择,指南没有明确的倾向,这里推荐阅读:观点:晚期肝癌一线和二线系统治疗推荐
二线治疗
目前推荐的方案还是获批的几个方案,包括瑞戈非尼、阿帕替尼、帕博利珠单抗、雷莫西尤单抗(血清 AFP≥400 ng/mL)、卡瑞利珠单抗和替雷利珠单抗。但因为这些方案都是基于索拉非尼治疗失败(少部分是化疗失败)的人群开展的研究而获得批准上市的,而现在一线治疗已经更新成了免疫联合治疗,所以这些二线治疗方案的适用性备受挑战。指南对于二线治疗的指导意见是:
对于一线接受免疫联合方案、免疫单药或酪氨酸激酶抑制剂单药治疗的患者,二线治疗方案选择可以考虑根据疾病进展方式和具 体一线方案不同,选择未曾使用过的一线治疗的药物或获批的二线治疗药物,鼓励患者自愿参加新药的临床试验。
这里推荐阅读:观点:晚期肝癌一线和二线系统治疗推荐